Aunque anteriormente hubo diferentes formas de clasificación de los elementos, no fue hasta 1869 con el joven ruso Dimitric Mendeléyev cuando se publicó la primera versión de la tabla periódica, la cual no sólo clasificaba y ordenaba a los elementos sino que también predecía que comportamientos podría tener aquellos elementos que aún no habían sido descubiertos. Posteriormente se demostró que muchas de sus predicciones eran correctas y se fue actualizando la tabla conforme aparecían nuevos elementos.
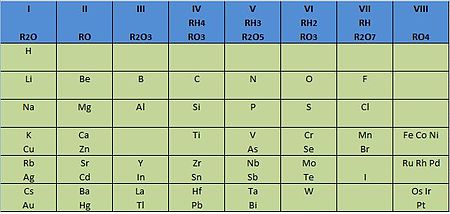
¿Para qué sirve la tabla periódica?
La función principal de la tabla periódica es ordenar los diferentes elementos según su número atómico, configuración electrónica y propiedades químicas, dejando así los elementos con comportamiento similares en la misma columna.
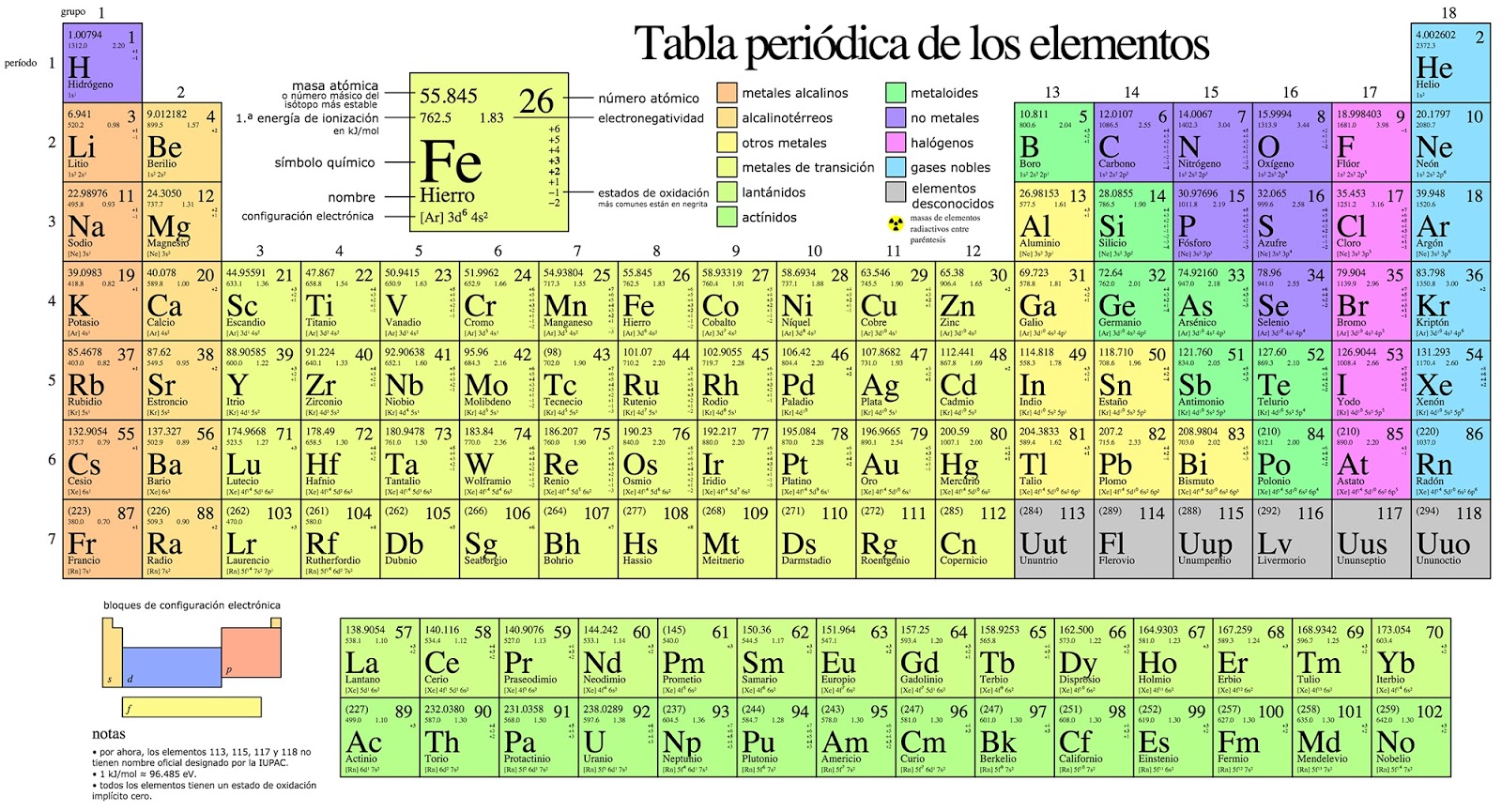
¿Cómo se ordena la tabla?
La tabla se distribuye en filas y columnas. Las filas se llaman períodos y formarán un total de 7, mientras que las columnas se denominan grupos siendo 18 en total. Hay grupos que tienen nombre propio como los alcalinos (grupo 1), alcalinotérreos (grupo 2), halógenos (grupo 17) , gases nobles (grupo 18).
Además la tabla se subdivide en 4 grupos según en que orbital se encuentre el último electrón de la configuración electrónica. Para ello debemos seguir el Principio de Aufbau, el cual nos va a indicar el orden en el que se van llenando los orbitales según sus niveles energéticos y por tanto donde se encontrará nuestro último electrón y el lugar que ocupará en la tabla.

Estos 4 subgrupos de la tabla serian s, d, p y f que son los distintos orbitales atómicos. Según la capa en la que se encuentre este último electrón, asi será su período.
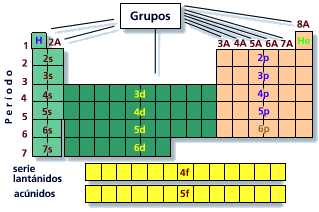
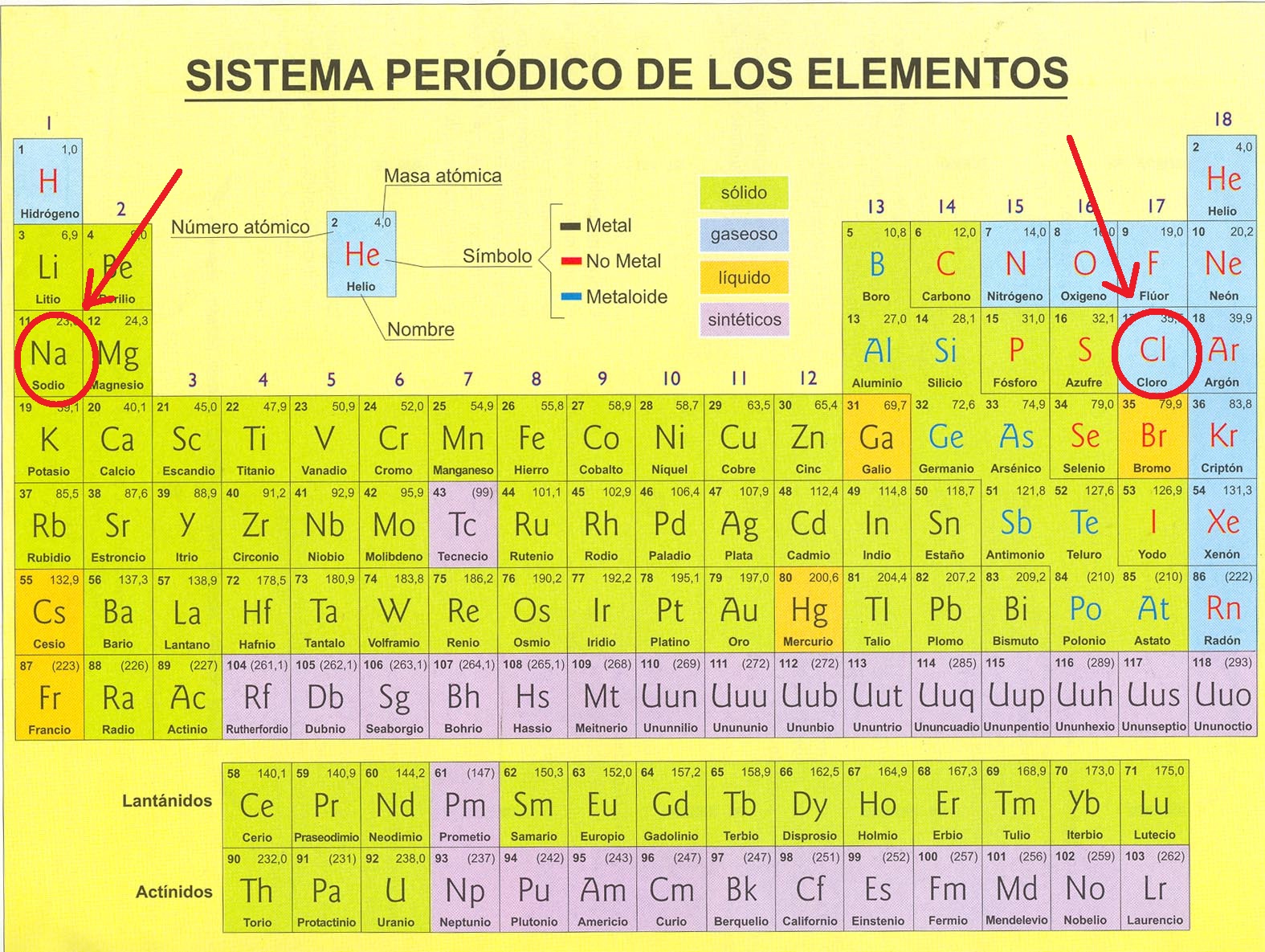
Por ejemplo, la configuración electrónica del Na es 1s22s2p63s1 . A nosotros nos interesa el 3s1 ya que esto significa que nuestro último electrón ocupa el orbital s1 por lo que estará en la columna 1 del grupo s, mientras que el 3 indica el período en el que se encuentra nuestro elemento. Por lo tanto ya sabríamos que lugar ocupa el Na en nuestra tabla periódica de los elementos.
El procedimiento es el mismo con todos los elementos, con el Cl [Ne] 3s23p5 (se utiliza la configuración electrónica de los gases nobles, en este caso [Ne], que les preceden como forma de abreviación) sabríamos gracias a su ultimo electrón, que se encuentra en el grupo 5 del orbital p en su período 3.

Muy interesante este artículo deberíamos de repasarla de vez en cuando.
Me gustaLe gusta a 1 persona
¡¡Me alegro que te haya gustado!! Y totalmente de acuerdo, no debemos olvidarla, ¡¡es muy importante!!
Me gustaMe gusta